논리화학의 최단경로 [2]
게시글 주소: https://i.orbi.kr/00038905343
개강 전까진 1주 2회(화/토 연재)로 바꿈.
개강후엔 쓰고싶을때 쓸듯
칼럼의 컨셉은 저번에도 말했듯이 '최단경로'임
'합리적이고 일관적이며 빠른' 풀이가 아니라 '최단경로'가 컨셉임을 유의하면 좋겠음
풀이가 좀 너무 발상적이라던가 내분을 너무 쓴다거나 그런 느낌이 들 수 있긴 할거임.
실제로도 시험장에서 모든 문제를 최단경로로 풀려고 하면 오히려 꼬이게 됨
그래도 적어도 기출문제에 한해선 최단경로 풀이를 혼자 생각해보고 알아두면 좋다고 생각해서 쓰기 시작한 칼럼임
칼럼 읽는 방법
1. 문제 사진을 보고 혼자 최단경로 풀이를 생각해본다
(혼자 안 풀어보고 풀이 감상만 하면 도움은 1도 안되고 오히려 독이 됩니다)
2. 자신의 풀이와 칼럼의 풀이를 비교 해 보고 자기가 더 빠르면 댓글로 단다
3. 혹시 최단경로 풀이를 보고 싶은 기출문제는 문항넘버나 문제 캡처한 사진을 댓글로 단다
여기서 최단경로 풀이는 답을 맞추는게 아닌 증명을 의미함
예를 들어 문제에서 케이스가 두 개면, 반대편 케이스가 틀렸다는 증명도 풀이에 들어가야함
그러니깐 잘찍어서 푸는 풀이로 풀어놓고 댓글다는 이상한 짓은 ㄴㄴ
오늘은 양적 3개, 중화 1개를 준비해옴
오늘 양적은 일차함수 그래프 유형을 컨셉으로 잡았음
비킬러는 선별하기가 애매해서 댓글로 원하는거 달아주면 그거 해 드릴게요

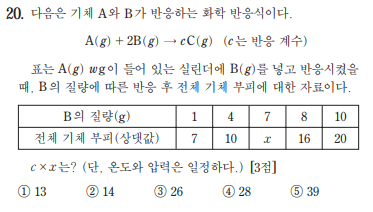
161120
스포방지용 간격
최단풀이
1. B의 질량 (1~4), (4~8), (8~10) 각각의 변화량은 3, 6, 4이고 기울기는 1, 1.5, 2임. 투입유형의 성질을 생각하면 기울기가 3개가 나오려면 (4~8)구간에 완결점이 존재함.
2. 기울기가 1, 1.5, 2 이므로 기울기를 내분 해 주면 완결점은 6(4와 8의 중점)일때임
3. 완결점 이후에 그래프 공식은 투입한 B의 질량을 t로 두면 y=2t이고, x(B질량 7)는 완결점 이후이므로 x=14
4. 기울기 공식 (c-a)/b를 사용하면 (c-1)/2:1=1:2에서 c=2. 답 28
마지막 c 구하기 다른 방법 : 완결점 이전 일차함수 공식은 y=t+6임
t=0일때 y=6, 완결점인 t=6일때 y=12이므로 전체 기체 부피 2배 -> a:c=1:2에서 c=2
추가설명
나머지는 스킵하고
기울기 내분 사용법 : 밀도 내분하듯이 기울기를 내분하면 됨
위 문제에선 기울기 1이랑 2를 걸친 평균 변화율이 1.5였으므로 1:1내분한것
물리 예시) 1차원 상의 어떤 물체가 4m/s로 운동하다가 10m/s로 속력을 바꿔 운동했는데, 평균속도가 8m/s이다. 총 운동시간이 6초라면, 4m/s로 운동한 시간은?
풀이 : 8의 4와 10에 대한 내분비는 2:1임. 따라서 시간 비는 역수이므로 1:2, 4m/s로 운동한 시간은 2초

190919
스포방지용 간격
이건 최단루트를 완벽히 이해하면 암산까지 가능한데, 대신에 중간중간 생각할게 좀 있고 일반적인 풀이 같지는 않음
최단루트
1. 그래프의 기울기가 완결점 전후 -3:1이므로 기울기 공식에 의해 a=5를 얻음.
2. 초기 부피가 y이므로, 완결점(B 5w)에서의 부피는 계수 비에 의해 2y/5
3. 반응 계수비를 보면 B:C=1:2이므로 이때까지 투입한 B의 부피는 y/5이며, 이게 5w의 부피임을 알 수 있음. 즉 B w당 부피가 y/25
4. 따라서 B 8w지점에서 전체 기체 부피는 2y/5 + 3y/25 = 13y/25. 이게 26이므로 y=50
5. B w당 부피가 y/25=2L이므로 B 20w당 부피가 40L, 즉 B 분자량 x=20w. 답은 5/2w
다른 최단루트
1. 기울기 공식에 의해 a=5
2. 0w지점에선 전체 기체 부피가 y. 계수 비에 의해 5w지점에서 전체 기체 부피는 2y/5
3. 일차함수니깐 내분으로 4w지점의 값을 구하면 됨. y와 2y/5를 4:1 내분하면 (5y+8y)/25=13y/25. 이게 26이니깐 y=50.
4. 완결점에서 부피는 20인걸 알 수 있고, B 3w를 넣었는데 6L증가했으므로 B 20w당 부피가 40L -> 분자량 20w. 답 5/2w

200720
스포방지용 간격
설명 포함 최단풀이
0. 주의할점 : 미리 반응을 어느정도 시킨 상태에서 더 반응시키는 상황임 낚이면 안됨
1. (0~w), (w~2w), (2w~3w)의 변화는 -6, -2, 2. 구간 길이 같으므로 이걸 평균 변화율로 둬도 무방하며, 기울기가 세개가 나왔으므로 앞선 문제와 같은 논리로 완결점은 (w~2w)에 존재함
2. -2는 -6과 2의 중점이므로 기울기 내분 하면 완결점은 1.5w
3. 기울기 비가 완결점 전후 -6:2=-3:1이므로, 기울기 공식을 사용하면 a=5
4. 1.5w에서 전체 기체의 부피는 완결점 이전이나 이후의 기울기를 이용해서 계산하면 12, 계수 비에 의해 시작할 때 부피는 30
5. 21은 30과 12의 중점이므로, 과정 (가)에서 1/2반응지점까지 반응시킨 후 (나)에서 계속 B를 투입했다는 것을 알 수 있음.
6. 1/2반응지점까지 반응시키려면, A의 초기 부피가 30이므로 B는 부피 3 만큼 넣어주면 됨(6개 넣으면 완결점이니깐 절반 반응지점은 3개넣으면 됨). 따라서 n/m=1/10, a랑 곱하면 1/2
요약 : 기울기공식쓰면 a=5, 내분하면 완결점 1.5w, 1.5w일때 부피 12니깐 시작할때 부피 30, 21은 30이랑 12의 중점이므로 (가)에서 1/2반응지점까지 반응시킴, 따라서 m:n=10:1. 끝.
여기까지 포인트 : 일차함수 그래프 유형은 내분을 은근 많이 쓰게 된다. 잘 분석해보자

210920
스포방지용 간격
일단 들어가기에 앞서서 이 문제는 많은 학생(심지어 강사들 마저) 논리적 비약을 하며 풀고있음
다들 첨가한 산 용액의 부피가 V일때 (나)의 몰농도가 (다)보다 작으므로 (나)가 2가를 투입했다~이런 소리를 하는데
너무 당연한 반례 하나를 들면, 만약에 이 시점에서 (나)랑 (다)가 둘 다 산성이면 작은 쪽이 1가를 투입한거임
(나)에서 V일때 염기성이니깐 가능하지 않냐고 물어볼 수 있는데
(다)가 V일때 산성이면 또 모순 만들 수 있음
제대로 된 논증은 (나)와 (다)가 둘다 염기성이다 -> 중화점 이전에 1가 산을 투입하면 이온 수는 안변하는데, 2가 산을 투입하면 개수가 감소한다->따라서 (나)가 2가를 투입했다 이거임.
암튼 최단풀이
0. 염기성 용액에 산성용액 한 종류를 일정하게 투입하면 모든 이온의 몰 농도 합 그래프는 무조건 감소하다가 증가하는 개형을 가진다는 것을 상기하자(만약 산성용액 두 종류를 투입하면 감소하다가 일정하거나, 계속 감소하는 그래프 개형을 가지는 것도 가능함)
1. (나)에서 V와 3V일때 모든 이온의 몰 농도 합이 같으므로, 개형을 떠올리면 V일때 염기, 3V일때 산성이다.
2. (다)에서 V와 2V일때 모든 이온의 몰 농도 합을 비교하면 V일때 더 크므로, V는 확실히 염기이고 2V일때 액성은 알 수 없다(만약 V가 산성이라면 2V일 때 모든 이온의 몰 농도 합은 증가해야함)
3. (나)와 (다)가 V일때 둘 다 염기성이므로, 모든 이온의 몰 농도 합이 더 작은 (나)가 2가 산을 투입한 상황이다
----------------논증파트 끝--------------------
1. (다)에서 투입한 HA가 0ml, Vml일 때 모든 이온의 개수 합이 같아야 하므로 1*10=(V+10)*3/5을 풀면 V=20/3
2. (나)에서 3V(=20)ml을 투입했을때 이온의 양은 1/2 * (20+10)=15mmol. 2가 산과 1가 염기의 혼합이고, 액성은 산성이므로 15mmol의 1/3인 5mmol이 B2-의 양
3. HA와 H2B의 몰농도가 같으므로 (다)의 3V 시점에서 A-의 양도 5mmol
4. 반응 초기에 모든 이온의 양은 10mmol이므로 Na+의 양은 5mmol임. 즉 (다)의 3V시점에서 용액은 중성. 모든 이온의 양은 여전히 10mmol
5. 따라서 10/30=1/3이 답
설명 하나 : 2가 산과 1가 염기의 혼합 상황에서 염기일때, 산성일때 모든 이온의 개수 합 공식은 그냥 외워두자
산을 x개 염기를 y개 넣었다 치면
만약 산성이면 전체 개수는 3x가되고
만약 염기면 전체 개수는 2y-x가 됨
이걸 더 확장한 공식이 있긴 한데 내책에 있음 대충 캡쳐해옴


0 XDK (+0)
유익한 글을 읽었다면 작성자에게 XDK를 선물하세요.
-
전역하고싶어 3
-
고 1
고
-
수학:96 영어:98 물리:46 지구:44 나름 자랑하는건데 씹갓들에 비하면... 부끄럽네요ㅜ
-
젠장 또 하니야 5
기습숭배
-
비추임?
-
금연 포기 0
두달 시도했는데 그냥 입시 끝나고 끊는게 맞는듯 ㅋㅋ
-
언니 장수생인데 아빠가 대학붙고 바로 공무원시험준비 하라니까 7
어제 싸우고 오늘도 계속 울던데 아빠가 잘못한건 아니지않나요? 성적도 어느정도 잘...
-
흠흠...
-
강남대성학원 재수종합반, 두각학원 단과 출강하시며 강남대성수능연구소에 계신...
-
1배속하면 말이 너무 느림. 현강 들을땐 안어색한거보면 인강으로 올릴 때 자체...
-
그래? 알앤디 한번 삭감했더니 문과가 살아나네!
-
다들 성적상승 1
계단식으로 오른다는걸 언제 어떻게 느껴보셨나요?
-
이매진 0
이매진이 연계 전작품 다있다는데 이거 8호까지 다풀고 복습하면 연계 충분한가요?
-
번호딸까
-
시기상 다들 힘 빠지고 의욕을 잃어갈 듯합니다... 다들 8월까지만 버티면...
-
문제에서 ㄱ보기가 옳다고 되어있는데 사내 동호회는 공식조직이 아니고 자발적 결사체...
-
지구에서 움직이는 우주선의 시간을 측정랄 때 지구의 시간은 지연된 시간이고 우주선의...
-
수특에 이렇게 나와있는데 그래서 답이 왜 3번인 거죠? 맨틀 위에 떠 있는 지각이래매...
-
지금까지 정부 스탠스상 진짜 당장 목에 칼 안들어오면 무조건 시간 끌거라고 봄...
-
소요 시간 72분 93점(독서 -5 문학 -2) 난이도는 6모랑 대비해서 독서는...
-
요새 강남 대치 부모님들 수능 성적표 달라고함? 과외힐때 3
보현사건땜에 달라하나? 이제
-
상남자 특 3
듄 연계공부 안함
-
문학 << 불 언매 << 불 비문학 << 가나형에 난이도 몰빵이 메타인건가 다 그런 느낌이네
-
파일 받아서 풀어봤는데 62점 나왔어요 교육청, 평가원에서는 대부분 2등급 받았어요...
-
잇올같은데 10월말 11월초에 3주정도 등록가능한가요..? 0
혹시 저때 등록해보신분 계신가요..?
-
몇 개 정도 푸시나요? 지금 구매한 게(상상, 이감, 김승모) 35~6회 정돈데 더...
-
아
-
스카 너무추워서 5
알래스카온줄 하하하
-
그래도 8시간은 했네..
-
어려운 27번 정도임?
-
멘탈관리법 1
여러분만의 멘탈관리법+정신건강유지법 공유해주세요..
-
이게 제일 어려운 듯 발표 중에서 자료 없이 쌩으로 5분 하는 게 존나 어려움...
-
꿈속에서 시간을10시로 착각해서 겁나 놀래가지고 진짜 일어났는데 아침8시였다
-
언매질문 3
왜 ㄱ 에 2,3번이 맞는게 아니라 1,4,5가 맞는건지 아무리 봐도 모르겠음 묻-...
-
기대기대
-
느낌이 옴
-
문학 인강 1
올오카 문학을 들었는데도 문학을 너무 못하고 문학은 김승리쌤이랑 안 맞는거 같아서...
-
훌륭한 마법사가 되겠어~
-
원하는 조건은 1. 특정 앱 몇개만 잠금or 특정 앱 몇개 제외하고 전체 잠금 가능...
-
강원대 의대 조사해보니 티오(?)도 낮고, 인기과 가기 힘들다고 하더라고요. 그래서...
-
와잉감자 부활 3
헿
-
고2입니다 이제까지 영어공부 제대로 해본적이 없구요 중학교때 부터 영어를 놔서...
-
서바 답지 0
서바 생명 라이브 듣고있는데 아니 답을 안알려주는데 어떻게 아나요??? 2회 답 알려주실분 없나요
-
언매 퀴즈 13
'강마르다'는 강조의 의미를 가진 접두사가 붙은 동사이다. (O, X)...
-
1번 자리- 옆뒤로 사람들 있음(성인 자격증,취업 준비로 추정됨) 2번 자리-...
-
나비효과 독서 0
이거 지금 봐도 딱히 의미 없을 것 같네 내가 직접 공부 좀 하고 문풀 어느정도 한...
-
기출을 아직 못돌려서 너기출이랑 같이 할 거를 찾고 있습니다. 현재 김기현 아이디어...
-
삼겹살이나 구워서 불닭이랑 같이 먹어야지
-
ㅈㄱㄴ
-
2.7 반택 9월달분까지만으로 팝니다 진짜





















































190919 a=5 안쓰는 풀이 하나 얹자면
0,0 5w,x를 이어주면 전 후 기울기가 2:1
13w=26이 나오고, 26이 y와 20을 4:1내분점이라 y=50을 구하는 방법.
그런데 a=5가 뻔히 보이는데 안찾고 푸는게 넌센스긴 하죠 ㅋㅋ
210920 V = 20/3 안구하는 풀이 하나 얹자면
액성 구한 후
V지점에서 이온 수 비가 6:5
중화점에서 이온 수 비가 4:3이니까 1.5V에서 2가 중화 -> 3V에서 1가 중화
1가 염기에 산 용액 첨가, 혼합용액이 산성일때 전체이온수 = 첨가한 산 이온수
따라서 3V지점 이온수비는 3:2
y=1/3
그런데 위랑 마찬가지로 V=20/3이 보이는데 안구한다는게 넌센스라 너무 뒷북스러운 풀이
첫번째껀 처음보네용
두번째껀 알고는 있었는데 까먹고 안 적었네요ㅋㅋ 근데 안구하는게 넌센스긴하죠 풀이시간 비슷하기도 하고

논화!논화!논화!논화!논화!6평 18번같은 순한맛 양적 빨리 푸는 방법이 궁금해요.. 그 문제를 19번보다 더 오래걸린듯

와 너무 유익해요!